
實驗大小鼠的(de)遺傳質量控製和遺傳監測: 標(biāo)準化實驗大小鼠分類
齧齒類實驗動物的遺傳質量控製應該(gāi)和微(wēi)生物質量控(kòng)製一樣作為(wéi)實驗動物(wù)設施質量控製計劃的重要組成部分。
本文由FELASA實驗小鼠遺傳質量控製(zhì)和遺傳監測工作組提出,描述了動物設(shè)施齧(niè)齒類動(dòng)物遺傳質量(liàng)控製計劃的目標和可用(yòng)方(fāng)法。
遺傳質量控製計劃的主要目標是:
(a)驗證近(jìn)交係及亞係(xì)的真實性和一致性,從而確保遺傳上的可靠(kào)性;
(b)檢測可能的基因汙染;
(c)精確描述遺傳係的遺傳組成。
雖然本文主要關(guān)注小鼠和大鼠的遺傳質量控製,但這些(xiē)原則也適用於其他齧齒類動物。
(一)標準化實驗齧齒類動物
01、近交係
國際小鼠標準化遺傳(chuán)命名委員會和大鼠基因(yīn)組命名(míng)委員對近(jìn)交係的定義(yì)是:一個品係經曆了至少連續20代的兄弟姐妹交配或親子交配,且品(pǐn)係內所有個體都可追溯到起源於第(dì)20代或(huò)以上代數的一對共同祖先,即為近交(jiāo)係。
此時,種群內的動物平均剩(shèng)餘雜合度≤2%,個體可視為基因相同(tóng)。據估計,兄弟姐妹交配需要24代才能達(dá)到雜合度< 1%,需要36代才能達到(幾乎)完全同源。
同源性意味著相同的組織相容性(xìng)(抗原),意味著品係內每個個(gè)體的基因都相同,一個品係的任意個體可以永久接受(shòu)來自同一品係和(hé)性別的任何個體的組(zǔ)織移(yí)植(zhí)。與克隆(lóng)動物和同卵雙胞(bāo)胎(所有基因組位點100%相同)不同,近交係齧齒類動物除了是等基因的,在幾乎所有的基因組位點上也都是純合子。
總的來說,每個近交(jiāo)係都代表一個隨機但獨特的(de)等位基因組(zǔ)合。如果用同樣的初始動物從零開始重新培育一個品係,經過同樣的20代(dài)近親繁殖,所產生的(de)品係在遺傳上一定不同於原來產生的那一個(gè)。
常見的(de)近交係小鼠品係(xì)包括(kuò):A/J、BALB/c、C3H/He、C57BL/6、DBA/2、FVB/N等;大鼠品係(xì)包括:ACI、BN、F344、LE、WKY等。
02、遠交係
遠交係是指(zhǐ)在一固定的群體內,以非近親交配方(fāng)式育成(chéng)的動物品係(xì),且連續15 代不從外(wài)部引入新的(de)動物種群。
遠(yuǎn)交係(xì)不同於近交係,因為它們的(de)基因是異質的(de),也就是某一動物的遺(yí)傳結構是從(cóng)這個遠交係(xì)遺傳基因庫中隨機(jī)抽取的,而不是已知的(de)。不過,一個遠交係群體中的所有動物都具有相同(tóng)的群體特征,例如白化病。遠交群(qún)具有良好的繁(fán)殖能(néng)力及與其他品係相比相對(duì)溫和等優點;這些特征使(shǐ)得這些(xiē)動物成為(wéi)輔助生殖(zhí)實驗中(zhōng)代孕母(mǔ)鼠的優質候選動物。
遠交係小鼠有ICR (CD-1)、CFW和NMRI(都(dōu)是從Clara J. Lynch於1926年進口到美國的原始“Swiss”小(xiǎo)鼠衍生而來)和(non-Swiss)CF-1。遠交係大鼠有Sprague Dawley (SD)、Wistar (WI)和Long-Evans (LE)。
由於遠交係在遺傳上的多樣性,通(tōng)常基(jī)於評估預期的表型性狀來做遺傳質量控製,如基於商(shāng)業繁(fán)育的大型群體(tǐ)通過基礎數據分析動物的毛色、生長和(hé)繁(fán)殖特征等(děng)信息來(lái)完成遺傳監控。由於遠交係和人類群體一樣是(shì)異質的,它們經常被用於毒理學和藥理學研究。然而(ér),也有(yǒu)遺(yí)傳學家對(duì)這樣的應用(yòng)提出了質疑,並批評了一些研究不恰當(dāng)地使(shǐ)用了(le)遠交(jiāo)係小鼠,在次優實驗中浪(làng)費了動物的(de)生(shēng)命和寶貴(guì)的資源。
(二)其他標準(zhǔn)化(huà)品係的小鼠和大鼠
雜交一代(dài)小鼠(F1)是由兩(liǎng)個獨立的近交係雜(zá)交產生的,在親本係擁有(yǒu)不同等位基因的所有位點上都是雜合的。F1同窩仔鼠基(jī)因相同,具有組(zǔ)織相容性。
同源導入近交係(congenic inbred strain),也稱近交同類係,是由兩個品係雜交產生的:攜帶特定等位基因或染色體區域的供體品係和將接受該位(wèi)點的受體品係進行雜交,產生的F1後代回交到受體品係,鑒定出攜帶(dài)該等位(wèi)基因的後代,並再(zài)次回交到受體品(pǐn)係。通常這個過程需要重複10個或更多的連續代次(cì)(圖1)。重複回交(jiāo)會讓受體品係除(chú)了攜帶指定等(děng)位基因的染色體區域(yù)以外的的染色體逐漸取代供體品係(xì)的染色體。
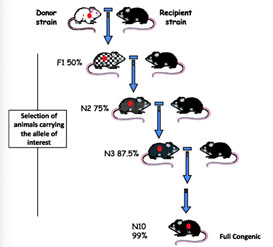
圖1:建立同類係的步驟
第一步是在攜帶(dài)特(tè)定基因的供體品係(例如,白化品係)和受體(tǐ)品係或背(bèi)景品係(例如,黑色品係)之間進行雜交。在每一代中,一個攜帶特定基因(*)的動物被回交給受體品係(遺傳連接基因被轉移,滲入片段的大小可以是數(shù)千或數百(bǎi)萬個堿基,並包括許多基因)。灰色的程度增加表明每回交一代後後代的背景基因組(zǔ)數量增加。當修飾後的基因沒有產生(shēng)易於識別的表(biǎo)型(例如(rú)皮膚或行為改變)時,就需要通過分子生物學方法做基因分型鑒定,以選出合(hé)適的載體(雜合)小鼠。
遺傳工程齧(niè)齒(chǐ)動物
通常有兩(liǎng)種不同的方法來表征基因功能(néng):
(1)正向遺傳學(從表型到基因型)旨在描述導致特定突變(biàn)表型的基因改變(通常來自自發(fā)或化(huà)學誘導(dǎo)突變)。
(2)反(fǎn)向(xiàng)遺傳學,旨在通過分析(xī)通常由研究人員(yuán)在DNA水平上設計的(de)在表型水平上顯現的後果來描述基因的功能。
本節簡單介紹了幾(jǐ)種獲(huò)得GA齧齒動物的基本方法:
(a)顯微注(zhù)射法,(b)載體(tǐ)介導的轉基因,(c)胚胎(tāi)幹細胞中的同(tóng)源重組,(d)基因編輯核酸酶,以及(e)化學誘導或自發突變。這些製備技術都有(yǒu)詳細描述並(bìng)已經公開發(fā)表,因此本文不作詳細(xì)描述。在(zài)使用基因編輯技術來創建轉基因動物之前,首先(xiān)應該檢查(chá)已有(yǒu)的數據庫來確定是否(fǒu)已經存在合適的動物模型,例如由傑克遜實驗(yàn)室(shì)和(hé)國際小(xiǎo)鼠表型聯盟管理(lǐ)的(de)數據庫。
(a)顯(xiǎn)微注(zhù)射法轉基因
首批顯微注射轉基因(yīn)小鼠誕生於20世紀80年(nián)代初。是(shì)將改造後的目的基因或基因組片段用顯微注射法注入供體小鼠的受精卵或著床前(qián)胚胎細胞,然後植入受體動物的輸卵管或子(zǐ)宮中,使其發育成攜帶有外源基因的轉基因動物(wù)。目前這種技術仍然被廣泛使用(yòng)。
該方法的整合位點是隨機的,因此容易造成基因(yīn)組(zǔ)重排(pái)、易位和缺失。還會出現多拷貝串(chuàn)聯整合,並導致外源(yuán)基因表達率低甚至不表達。
(b)載體介導的轉基因
通過逆轉錄病毒/慢病毒載體將外(wài)源基因連接到長末端重複(fù)序列下遊進行基因重組(zǔ)後,再包裝成高滴度病毒顆粒,直接(jiē)感染受精卵或顯微注射到囊胚(pēi)腔中,攜帶外源基因(yīn)的反轉錄病毒DNA就可以整合到宿主染色體上(shàng)了(le)。
除了逆轉錄病毒(dú)載體,預處理過的攜帶外源基因的精(jīng)子也被成功地用(yòng)作載體,在受精過程中將外源基因導入動物胚胎,從而獲得轉基因後代。
每種技術都有其優缺點,例如,病毒載體(tǐ)隻能(néng)導入較(jiào)小的(de)外源基(jī)因,而精子介導的轉基因技術則可能(néng)影響精子自身的遺傳物質質量。
(c)胚胎幹細胞同源重組靶向誘變
胚胎幹細胞介導法是通過(guò)將外源基因導入胚(pēi)胎幹細胞,然後(hòu)將轉入基因的胚胎幹細胞注射入受體動物胚胎後,可(kě)參與宿主的胚胎構成(chéng),形成嵌合體,直至達到生殖係嵌合,並形成子代(dài)。
(d)使用核酸酶進行基因編輯(jí)
在過(guò)去十多年中,一些新的技術越來越廣泛地應用於大小鼠(shǔ)和其他物種的靶向(xiàng)突變(biàn)。例如鋅指核酸酶技術、TALEN技術和CRISPR/Cas9技術等,特別是CRISPR/Cas9技術,利用sgRNA識別基因(yīn)特定靶序(xù)列,介導Cas9酶定位並剪切基因。當(dāng)同時加入同源重組模板時,即可達到基因(yīn)導入的目(mù)的。CRISPR/Cas9技術已被用(yòng)於基因敲入、敲除(chú)和點突變。該技術高度靈活、快速和高效,可以在任何遺傳背景(jǐng)下製造KO和KI係。
然而(ér),這項技(jì)術也(yě)需要進行廣泛的基因序列(liè)分析和篩選(xuǎn),以確保存在所需要的序列(liè),同時不存在非靶向突變或其他不可預測的更大的基因組改變。
(e)自(zì)發的和化學(xué)誘(yòu)導的突變
自發突變(biàn)可通過觀察異常的(de)表型發現,它(tā)有幾個優點:首先它們的產(chǎn)生幾乎不需要成本;第二,它們通常有明顯的表(biǎo)型(xíng);第三,自發突變代表(biǎo)了各種各樣的分子(zǐ)事件,如缺失、插入和點突(tū)變,不僅產(chǎn)生功能缺失的等位基因,還產生低形態和高形態的等位基因;最後(hòu),突變產生於各種背景,包括(kuò)近交係和遠交係(xì)。
經典的自發突變模型包括:裸鼠(shǔ)(Foxn1nu )、scid(Prkdcscid )、無毛(máo)小(xiǎo)鼠(shǔ)(Hrhr )、糖尿病小(xiǎo)鼠(Leprdb )、肥胖症小鼠(Lepob )和(hé)肌肉(ròu)萎縮症小鼠(Dmdmdx )以及(jí)Rowett裸大鼠(Foxn1rnu )和Zucker糖尿病脂肪大鼠(Leprfa )等。
乙酰基亞硝基脲(ENU)可作(zuò)為誘(yòu)變劑應用於小(xiǎo)鼠疾(jí)病模型的篩選。由於ENU通常產生點突變,它廣泛應用於正向遺傳篩選。ENU誘變(biàn)的主要缺點是它產生(shēng)的突(tū)變是(shì)隨機的而不是靶向(xiàng)突變。
參考文獻:
[1] Benavides F , T Rülicke, Prins J B , et al. Genetic quality assurance and genetic monitoring of laboratory mice and rats: FELASA Working Group Report:[J]. Laboratory Animals, 2020, 54(2):135-148.


